由保健食品新舊功能文件發(fā)布引發(fā)的行業(yè)思考
2023-09-15
《保健食品新功能及產(chǎn)品技術(shù)評價實施細則(試行)》《允許保健食品聲稱的保健功能目錄 非營養(yǎng)素補充劑(2023年版)》及配套文件的發(fā)布,將推動保健食品新功能及產(chǎn)品研發(fā),更好滿足人民群眾健康需求,保健食品行業(yè)監(jiān)管工作將進入穩(wěn)中求進、動態(tài)發(fā)展、鼓勵創(chuàng)新階段,至此,注冊備案雙軌制下以創(chuàng)新為驅(qū)動的保健食品全周期通路基本構(gòu)建完成,行業(yè)高質(zhì)量發(fā)展也有了可靠的抓手。
一、引領(lǐng)行業(yè)資源備案注冊雙管齊下
保健食品備案工作是在總結(jié)獲批保健食品配方、功能及工藝等基礎(chǔ)上,基于安全性、功效性及質(zhì)量可控性進行的標準化工作,換言之,注冊是備案的前提,備案是注冊的延續(xù)。
因此,保健食品備案工作的核心是標準,而保健食品注冊工作的核心是創(chuàng)新,隨著《保健食品新功能及產(chǎn)品技術(shù)評價實施細則(試行)》《允許保健食品聲稱的保健功能目錄 非營養(yǎng)素補充劑(2023年版)》及配套文件的發(fā)布,一方面提振了行業(yè)信心,另一方面也勢必會促成保健食品行業(yè)資源重新分配,引領(lǐng)部分保健食品企業(yè)(尤其是注重創(chuàng)新的企業(yè))的工作重心向注冊傾斜,向創(chuàng)新發(fā)力。
從保健食品主要法規(guī)來看,在新舊功能文件發(fā)布前,近2年內(nèi),正式發(fā)布及實施的均為備案相關(guān)法規(guī),說明了備案是標準化工作,難點是提煉、總結(jié)和梳理;隨著新法規(guī)的發(fā)布完善,也體現(xiàn)了雙軌制動態(tài)發(fā)展的趨勢,也從側(cè)面說明了注冊是創(chuàng)新性工作,需要審慎前行。

食品工業(yè)在國民經(jīng)濟占據(jù)著舉足輕重的地位,不僅與人民生活質(zhì)量、健康水平密切相關(guān),而且還是消費品工業(yè)中為國家提供積累最多、吸納城鄉(xiāng)勞動就業(yè)人員最多、與農(nóng)業(yè)依存度最大、與其他行業(yè)關(guān)聯(lián)度最強的產(chǎn)業(yè)。在“健康中國”國家戰(zhàn)略提出和實施的背景下,保健食品本應(yīng)承載更多的創(chuàng)新使命,接收行業(yè)源源不斷的創(chuàng)新需求。隨著新功能文件的發(fā)布,保健食品行業(yè)的創(chuàng)新有了明確的方向和通路,保健食品強基固本、守正創(chuàng)新,必將成為食品工業(yè)創(chuàng)新的“領(lǐng)頭羊”。
二、體現(xiàn)了保健食品管理改革和創(chuàng)新
新功能文件是從制度上改革我國以往保健食品功能聲稱評價管理模式的重要舉措,體現(xiàn)了我國保健食品管理的創(chuàng)新,在制度方面,將新功能及產(chǎn)品的非行政許可納入保健食品領(lǐng)域,并作為保健食品全周期管理的重要組成部分;在審評方面,創(chuàng)造性地提出了保健功能分級、功能及產(chǎn)品關(guān)聯(lián)審評及上市后評價等措施,擺脫常規(guī)工作思路,基于功能及產(chǎn)品的“新”,提出技術(shù)審評工作細節(jié)的“新”,以制度創(chuàng)新引領(lǐng)產(chǎn)業(yè)創(chuàng)新,以消費結(jié)構(gòu)升級引領(lǐng)產(chǎn)業(yè)轉(zhuǎn)型升級,從而實現(xiàn)保健食品產(chǎn)業(yè)的高質(zhì)量發(fā)展。
三、帶動保健食品及相關(guān)行業(yè)發(fā)展
專業(yè)化分工是現(xiàn)代產(chǎn)業(yè)發(fā)展的一種重要趨勢,對于推動經(jīng)濟發(fā)展和提高行業(yè)競爭力具有重要意義。保健食品新舊功能文件的發(fā)出,一方面會吸引更多的研發(fā)創(chuàng)新、臨床試驗及檢驗檢測等機構(gòu),或催生新的專業(yè)化服務(wù)機構(gòu),另一方面也擴大了保健食品行業(yè)“產(chǎn)學(xué)研”的合作與交流,提高效率、促進專業(yè)化發(fā)展、優(yōu)化資源配置、推動技術(shù)創(chuàng)新,拓展市場和增加就業(yè)機會。
具體到保健食品功能創(chuàng)新,新功能文件指出,將根據(jù)科學(xué)依據(jù)的充足程度,明確新功能保健食品的保健功能聲稱限定用語,分級標注保健功能聲稱為“①科學(xué)證據(jù)(非結(jié)論性證據(jù))/②支持性研究證據(jù)(非結(jié)論性證據(jù))/③有限的研究證據(jù)(非結(jié)論性證據(jù))表明產(chǎn)品具有***功能”,未來,將會有部分保健食品新功能加入到“①②③”行列,同時隨著產(chǎn)品上市后評價及科學(xué)、人群等依據(jù)的逐步充足,也推動著新功能由“②③”向“①”轉(zhuǎn)化,進而產(chǎn)生保健食品功能“金標準”,一方面提升了保健食品行業(yè)的整體素質(zhì),另一方面也為其他保健食品新功能評價方法提供了向“金標準”攀爬的梯子,以創(chuàng)新驅(qū)動行業(yè)發(fā)展。
四、構(gòu)建了保健食品全周期通路
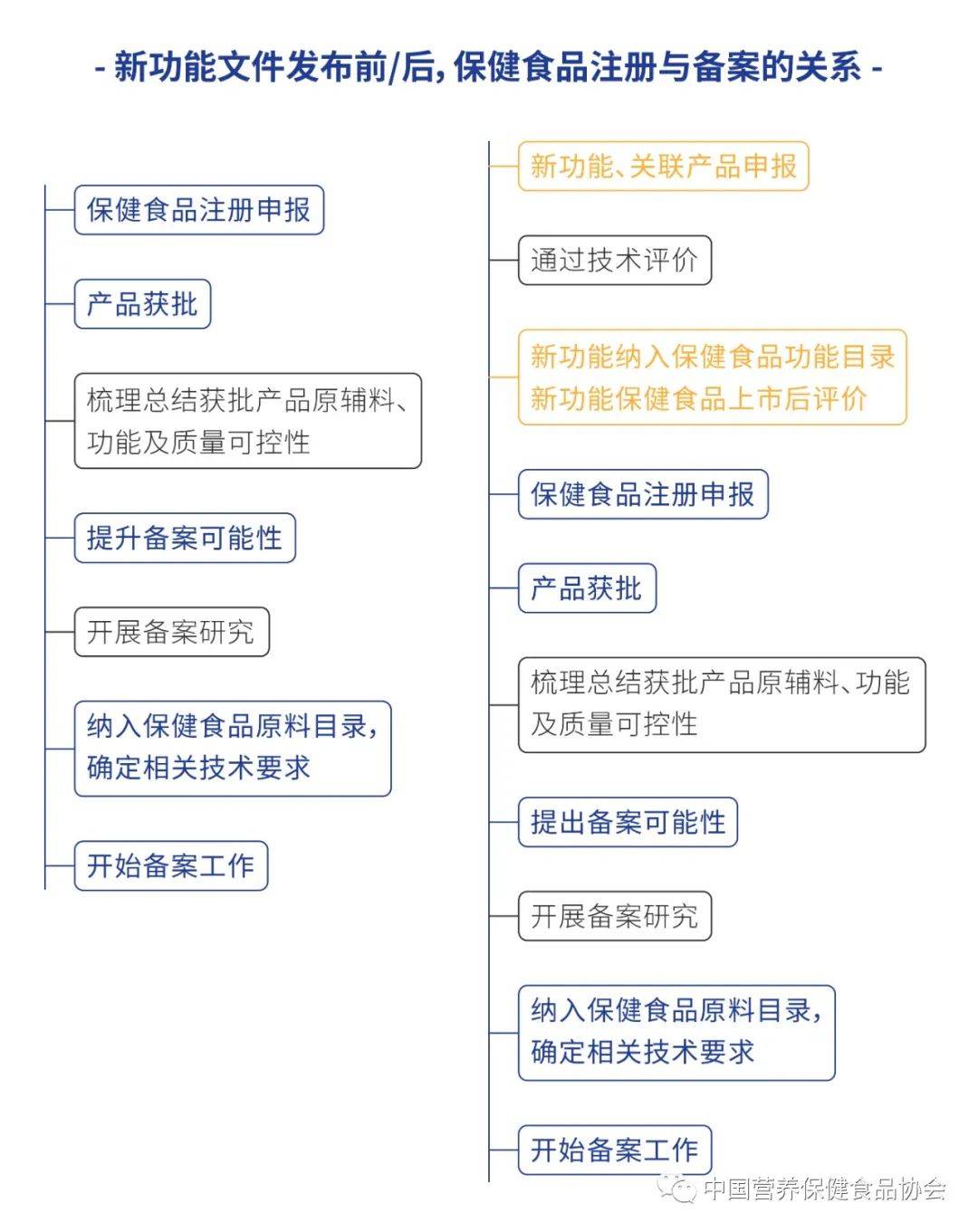
2019年10月1日,《保健食品原料目錄與保健功能目錄管理辦法》實施,對于保健食品功能目錄,缺少具體的申報、技術(shù)審評細則;對于保健食品原料目錄,也僅僅能從已獲批的、原功能的保健食品中去提煉、梳理和總結(jié),而缺少保健食品新功能及產(chǎn)品的源頭及通路。
2023年8月28日,《保健食品新功能及產(chǎn)品技術(shù)評價實施細則(試行)》實施,宣告著以創(chuàng)新為驅(qū)動的保健食品全周期通路構(gòu)建完成,自2016年7月1日保健食品注冊與備案雙軌制實施以來,保健食品行業(yè)迎來了全新的發(fā)展機遇。
五、保健食品有了“再繁榮”的基礎(chǔ)和底氣
三類特殊食品都有著嚴格準入的法規(guī)要求,各自也存在不同的特點。嬰幼兒配方食品、特殊醫(yī)學(xué)用途配方食品有明確的國標要求,準入環(huán)節(jié)是個性化特征和標準一致化的研究;保健食品由于存在漫長的歷史,對應(yīng)監(jiān)管部門和規(guī)章制度復(fù)雜,同時產(chǎn)品品類繁多,個體問題多樣,監(jiān)管法規(guī)建設(shè)道路漫長而艱難。行業(yè)發(fā)展也存在困難和疑惑。
新功能文件的發(fā)布,標志著保健食品創(chuàng)新側(cè)的邏輯和通路構(gòu)建基本完成,《允許保健食品聲稱的保健功能目錄 非營養(yǎng)素補充劑(2023年版)》及配套文件的發(fā)布,調(diào)整了功能表述、刪除了部分功能、規(guī)定了未在保健功能目錄產(chǎn)品的轉(zhuǎn)化路徑等,攘“舊”必先安“新”,保健食品有了“再繁榮”的基礎(chǔ)和底氣,未來,保健食品將雙向發(fā)展。
近期,保健食品法規(guī)文件密集發(fā)布,給保健食品行業(yè)帶來莫大的驚喜,讓大家驚呼“過年”。我們有理由期待,在煙花爆竹聲聲響之后,那盤“餃子”也能被盡快端上餐桌。
來源:中國營養(yǎng)保健食品協(xié)會